 9
9
生物兼容性是指材料与生物体之间相互作用后产生的各种生物、物理、化学等反应的一种概念]。一般地讲,就是材料植入人体后与人体相容程度,也就是说是否会对人体组织造成毒害作用。
1、对细胞没有毒性的试验
2、不会引起组织应变性或致敏性反应试验
3、对组织没有刺激性作用试验
生物学评估可按接触部位(皮肤、粘膜、组织、血液等)、接触方式(直接或间接)、接触时间(暂时、中期和长期)和用途分类,评估的生物学实验项目包括细胞毒性试验、致敏试验、刺激反应试验、亚急性毒性试验、植入试验、血液相容性试验、慢性毒性试验、致癌性试验、生殖与发育毒性试验、生物降解试验等。
细胞毒性/生长抑制试验(ISO 10993-5)
溶血试验(ISO 10993-4)
化学分析/“指纹图谱”试验(ISO 10993-18)
生物毒理学评估试验(ISO 10993-1)
采用此方法,恩欣格遵循了ISO 10993-1标准,逐步进行生物认证。
生物兼容性是指材料与生物体之间相互作用后产生的各种生物、物理、化学等反应的一种概念]。一般地讲,就是材料植入人体后与人体相容程度,也就是说是否会对人体组织造成毒害作用。
1、对细胞没有毒性的试验
2、不会引起组织应变性或致敏性反应试验
3、对组织没有刺激性作用试验
为了确保医疗设备的生物兼容性,根据ISO 10993-1 – ****套评估医疗设备生物兼容性的国际标准和FDA blue book memorandum (#G95-1),中提出了几项帮助医疗设备制造商选择材料的试验。 所有医疗设备均须通过细胞毒性、刺激和过敏三项测试。
通常包括组织相容性与血液相容性两大类:
组织相容性——涵盖细胞吸附性、无抑制细胞生长性、细胞激活性、抗细胞原生质转化性、抗类症性、无抗原性、无诱变性、无致癌性、无致畸性等;
血液相容性——是指能抗血小板血栓形成、抗凝血性、抗溶血性、抗白血细胞减少性、抗补体系统亢进性、抗血浆蛋白吸附性和抗细胞因子吸附性等。
生物兼容性指的是医用材料和病人的组织和生理系统间的相互适应性。医用材料能在临床安全使用,主要缘于其良好的生物兼容性标准通常包括的测试项目有体外细胞毒性测试、皮肤刺激性测试、致敏试验。
生物相容性测试,医用材料生物相容性测试,生物相容性检测可以选择亿博检测认证中心。医用材料生物相容性测试,深圳生物兼容性检测。
生物相容性的定义
生物相容性是指材料在特定的实际应用中引起适当的宿主反应和材料反应的能力.材料和生物机体的相互作用主要表现在两个方面,一是材料反应,即活体对材料的作用,包括生物环境对材料的腐蚀、降解、磨损和性质退化,甚至破坏
一般来讲,生物相容性就是指血液和透析膜或吸附剂等异体物质间的相互作用.当反应轻微,患者可耐受时,此种材料称为生物相容.目前透析膜所导致的急性血液动力学不稳定,自一些生物相容性较好的膜如血仿膜等的应用以来,已经明显减少
生物相容性是指所有材料设备、过样或系统对宿主不引起明显的临床反应,即尢血栓形成、无毒性、无过敏或炎症反应、无破坏血细胞作}}3,小激活补体
生物相容性是指机体*系统对外异物的反应及耐受能力.本试验表明动物机体对不锈钢丝制作的支架具有良好生物相容性支架置入后血管壁未见炎性及坏死改变
材料的毒性及生物相容性是评价新材料另一个必须考虑的问题,生物相容性是指材料与人体之间相互作用产生各种复杂的生物、物理、化学反应,以及人体对这些反应的忍受程度
所谓生物相容性是指血液和生物材料之间发生的特异性或非特异性反应.在HD过程中透析膜是引起生物不相容性反应的重要原因细胞因子与膜的生物相容性研究已日益受到重视
生物相容性是指在所需时间内,材料在体内或体外持续完成所需功能达到的能力.寺反明显,在大部分情况下,材料的优选标准和材料的失效原因一般属生物相容性的考虑范畴
航天检测提供生物相容性测试,包括,细胞毒性测试、致敏性测试、皮肤刺激性测试,欢迎来电咨询。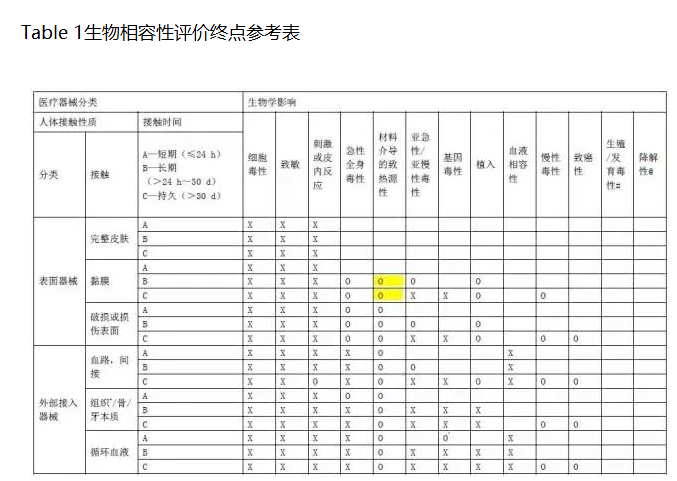
我司主要业务:
欧盟:CE :MD ,MDD ,EMC, LVD, PED ,PPE ,RoHS ,EN71, CPD ,RTTE
美国:FCC:VOD, DOC, ID 加州65 ,ASTM ,CPSC, CPSIA
日本:PSE ,TELEC
食品级:欧盟食品级, FDA ,LFGB
尼日利亚:PC SC 肯尼亚:PVOC 沙特:SASO 化学测试:Reach
美国法律标,TSSA注册,美*儿童打开测试ASTM-D3475,欧盟授权代表和自由销售证书
一、杀菌/抑菌效果验证实验
公司根据《消毒技术规范》的方法对各种具有消毒或杀菌作用的产品进行杀菌效果验证并出具检测报告。可以作为客户产品杀菌作用强有力的说明文件。
二、生物相容性试验
医用材料和病人的组织和生理系统间的相互适应性。
生物相容性测试的项目有很多,通常较常测的有三个项目:
细胞毒性试验:
医疗器械生物学评价*5部分:体外细胞毒性试验GB/T 16886.5
医疗器械生物学评价*10部分:刺激与迟发型**敏反应试验GB/T 16886.10
致敏试验:
医疗器械生物学评价*10部分:刺激与迟发型**敏反应试验GB/T 16886.10
三、毒理试验
毒理检验对保证食物、化妆品和化学产品安全具有重要作用。通过动物实验和对人的观察,阐明某一化学物的毒性及其潜在危害,以便为人类使用这些化学物质的安全性作出评价,为制订预防措施特别是卫生标准提供理论依据。
评价的步骤:目前我国现行的对食品安全性评价的方法和程序也还是按照传统的毒理学评价程序:即初步工作→急性毒性试验→遗传毒理学试验→亚慢性毒性试验(9d喂养试验、繁殖试验、代谢试验) →慢性毒性试验(包括致癌试验)(GBl5193.1—94)。